新冠疫苗获批上市前,许多研究者都希望单克隆抗体可以发挥作用,减少重症病人和住院人数的增长。然而,虽然FDA已经授予新冠中和抗体紧急使用授权(EUA),但由于其局限性临床使用中这类抗体的用量却很小。
首先,新冠抗体的治疗窗口期不长,通常仅在疾病过程前的4-7天内使用才有效。其次,大流行期间患者激增,医务人员缺乏,药物无法及时被用于患者。此外,变异毒株的表面刺突蛋白变异也可能致抗体疗效下降等。因此,我们需要一款可以有效应对变异毒株并且不需要静脉注射的抗体药物。
纳米抗体的作用方式
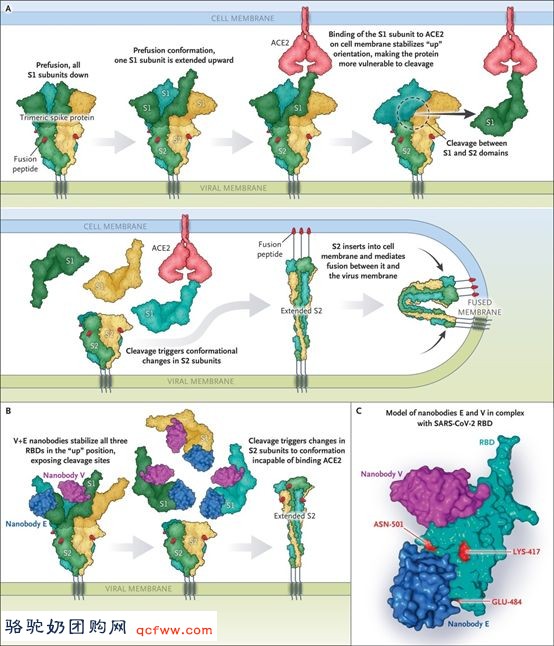
新冠病毒(SARS-CoV-2)刺突蛋白由亚基1 (S1)和亚基2 (S2)组成。三聚体刺突蛋白在病毒表面表达(图1A)。在融合前构象中,一个S1亚基向上延伸。S1亚基与细胞膜上受体蛋白血管紧张素转换酶2(ACE2)的结合稳定其“向上”的方向,从而诱导蛋白水解和分离。此分离引发S2亚基的构象变化,使融合肽延伸到宿主细胞膜,于是宿主细胞膜和病毒膜通过S2亚基相结合。
V+E纳米抗体将三个表面刺突糖蛋白受体结合区(receptor-binding domain, RBD)稳定处于“向上”位置。这种稳定结构促使蛋白水解和早期的结构转化的发生,但不会导致膜的融合(图1B)。纳米抗体V和E与新型冠状病毒的RBD(蛋白质7KSG和7KN6)形成了复合体结构(图C)。红色代表B.1.1.7和B.1.135变体的氨基酸(K417,E484和N501)。
骆驼科动物衍生的单结构域抗体(或纳米抗体)具有很多的优点。研究人员采用新型冠状病毒的刺突蛋白作为抗原刺激羊驼和美洲驼的免疫系统,然后在动物体内分离出与病毒表面刺突糖蛋白受体结合域(RBD)特异性结合的纳米抗体。
研究人员通过多种体外试验对四种具有中和作用的纳米抗体(代号E、U、V和W)的结构和功能进行了表征。三个纳米抗体(U、V和W)识别位于融合前的刺突蛋白三重轴附近的一个共同表位,而纳米抗体E识别与RBD重叠的延伸环(残基R466至P491)(图1C)。
纳米抗体与病毒的受体结合区结合的平衡解离常数为2-22nmol,并在48-185nmol的浓度范围内可以消除50%的新型冠状病毒感染。与纳米抗体V相反,纳米抗体E,U和W具有阻止SARS-CoV-2结合宿主细胞上的ACE2的可能性,这与它们结合表位的位置以及它们与细胞表面RBD的结合方式有关。纳米抗体通过诱导融合前构象到不可逆融合后构象的早期结构转变来抵御病毒,后者(即不可逆融合后构象)不能结合ACE2,因此不能触发膜融合。
之后,研究人员通过基因工程技术将靶向不同表位区域(例如E+ V,V+ E,E+ W和W+ E)的纳米抗体基因融合,表达出双特异性纳米抗体(即在一个分子中具有两个抗原结合位点的纳米抗体)。
使用冷冻电子显微镜技术可以发现双特异性纳米抗体(V+E)与病毒表面的三聚体刺突蛋白相结合紧密,稳定了受体结合区,并防止其上下运动,导致刺突蛋白水解,转变为不可逆的融合后构象。
可能是因为和刺突蛋白亲和力的显著提高(亲和力比单个纳米体高至少22倍),V+E双特异性纳米抗体在比单个纳米抗体低62倍的浓度下仍然可以抵御新型冠状病毒的感染。
研究者们发现,当存在纳米抗体E,U,V和W的情况下在VeroE6细胞中传代的嵌合病毒表位区域会发生突变,从而逃逸抗体的识别。相反,在双特异性纳米抗体(V + E或E + V)的存在下,传代的嵌合病毒不会发生这种表位区域内的“逃脱突变”。该观察结果强调了同时靶向多个表位的优势。
值得注意的是,V纳米抗体的结合位点并不包含刺突蛋白的氨基酸417、484和501(图1C),这一突变体在英国,南非和巴西最近发现的菌株中都有,因此双特异性纳米抗体V+ E(或E+ V)将对这些突变体仍然有效。
纳米抗体的优势
纳米抗体分子量相对较小,拥有良好的生物物理特性,并且生产成本低于标准单克隆抗体。
首先,它们的小尺寸和长的重链互补区使它们能够靶向凹形表位,例如刺突蛋白的受体结合区。其次,纳米抗体可以使用原核表达系统(例如细菌或酵母)来制备,因为它们不含糖基化的Fc结构域,使得它们比标准单克隆抗体更容易制备。再次,Fc结构域的缺失消除了抗体依赖性感染增强的风险,但也缩短了纳米抗体的体内半衰期,不过可以通过聚乙二醇化或结合人血清白蛋白的方法提高半衰期。最后,纳米抗体可以通过吸入雾化给药,直接到达新冠肺炎患者的肺部,从而替代静脉注射抗体。在非临床研究中,纳米抗体的气溶胶制剂已经显示出富有希望的结果。
展望
尽管治疗癌症和传染性疾病等多种疾病的纳米抗体还处于临床研究中,但欧洲药品管理局(EMA)和美国食品药品监督管理局(FDA)批准了卡拉西单抗(caplacizumab,一种抗血管性血友病因子二价纳米抗体)用于治疗血栓性血小板减少性紫癜和血栓形成,这标志着纳米抗体已进入治疗领域。
双特异性纳米抗体V+E的结构形式虽然不同于传统的纳米抗体,但与FDA批准的基于单链可变片段的双特异性抗体博纳吐单抗相似(图2)。因此双特异性抗体可能为新冠肺炎的治疗提供一种比常规单克隆抗体更好的治疗药物。

图2,双特异性血红蛋白抗体和新型冠状病毒双特异性纳米抗体的模块化组织。
图中显示了双特异性博纳吐单抗(blinatumomab)(上)和新型冠状病毒纳米抗体V+E(下图)的结构。在博纳吐单抗中,CD19抗体的单链可变片段是通过5个氨基酸相连形成的短链肽与CD3抗体的单链可变片段相连(上)。新型冠状病毒双特异性纳米抗体的结构与单链可变片段的结构相似:它是由两个驼科的单结构域(重链)抗体(即两个纳米抗体)通过15个氨基酸的连接肽相互连接而成(下)。两种抗体都缺乏可结晶的Fc结构域。VH表示重链可变区,VL表示轻链可变区。
最近,来自于包括监管机构,学术界以及制药和生物技术公司的专家们呼吁开发抑制病毒复制机制的小分子药物。小分子药物给药方便,对病毒突变不敏感。而双特异性抗体配制成气雾剂或经皮下给药时,双特异性抗体将同样具备小分子药物的优势。